24 март 2026 г. отбелязва 31-ия Световен ден за борба с туберкулозата. Световната здравна организация (СЗО) обяви тазгодишната глобална тема като„Да! Можем да сложим край на туберкулозата!“, като подчертава, че силното правителствено лидерство, трайният политически ангажимент и координираните многосекторни действия са от съществено значение за прекратяване на епидемията от туберкулоза (ТБ).

Глобален напредък и оставащи предизвикателства
Според Глобалния доклад за туберкулозата за 2025 г., глобалният контрол на туберкулозата е постигнал важен етап през 2024 г., като и двете...заболеваемостта и смъртността намаляватза първи път от пандемията от COVID-19 насам.
Приблизително10,7 милиона душиразвиха туберкулоза през 2024 г., включително 54% мъже, 35% жени и 11% деца и юноши. Сред тези случаи приблизително619 000 (5,8%)са били коинфектирани с ХИВ и390 000 (3,6%)са били мултирезистентни или рифампицин-резистентни туберкулози (MDR/RR-TB).
Туберкулоза, причинена от приблизително1,23 милиона смъртни случаяпрез 2024 г., оставайки водещата инфекциозна причина за смърт в световен мащаб, изпреварвайки COVID-19. След три години на увеличение между 2021 г. и 2023 г., световната честота на туберкулозата е намаляла с близо 2% през 2024 г., което отразява постепенното възстановяване на услугите за туберкулоза.[1]
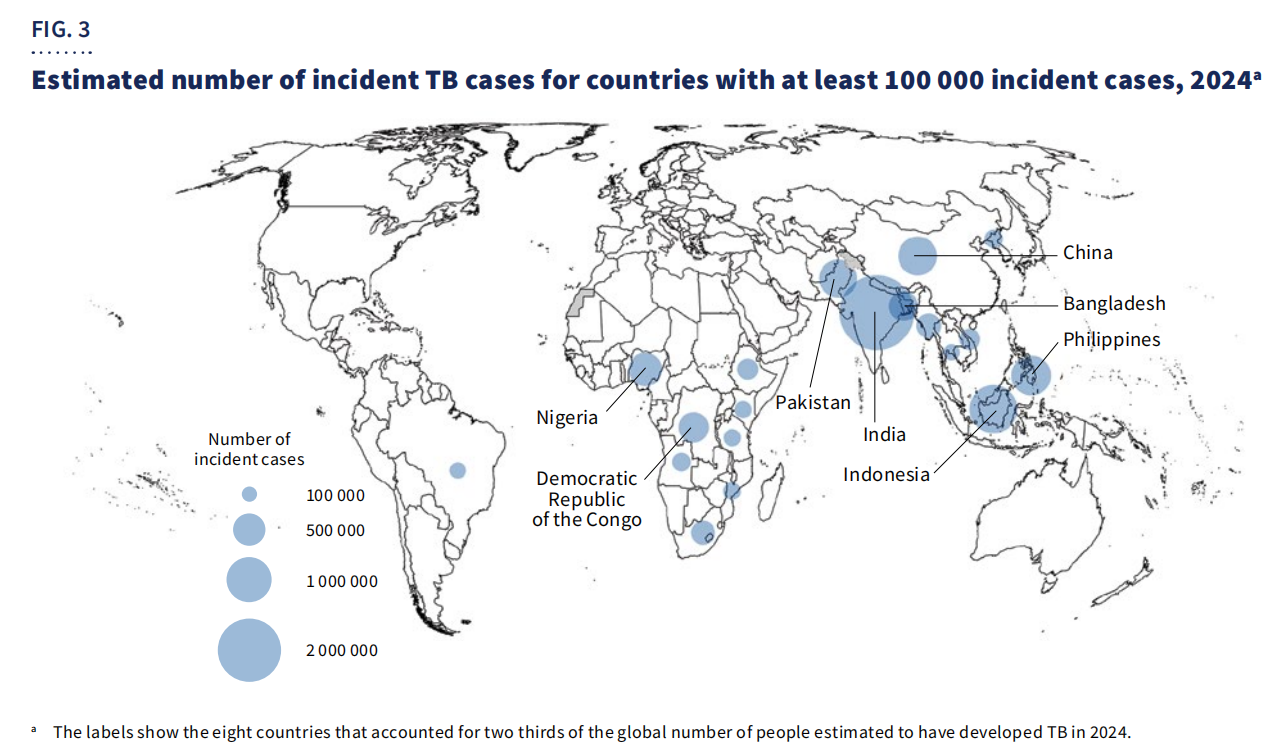
Географски,67% от случаитебяха концентрирани в осем държави: Индия, Индонезия, Филипините, Китай, Пакистан, Нигерия, Демократична република Конго и Бангладеш.
Въпреки напредъка, туберкулозата остава водеща причина за смърт сред хората, живеещи с ХИВ, и основен фактор за смъртността, свързана с антимикробна резистентност. Глобалното финансиране продължава да е недостатъчно, като само5,9 милиарда щатски долараналични през 2024 г. – далеч подГодишна цел от 22 милиарда щатски долараопределен за 2027 г.
Тези цифри подчертават спешната необходимост от укрепване на програмите за контрол на туберкулозата в световен мащаб, с акцент върху разширяване на достъпа до диагностика, подобряване на резултатите от лечението и справяне със социалните детерминанти, които стимулират предаването на туберкулозата. Туберкулозата продължава да изисква стабилно международно сътрудничество и политически ангажимент за постигане на целите на Стратегията за премахване на туберкулозата.
Mycobacterium tuberculosis: Патогенеза и класификация
Mycobacterium tuberculosis (MTB/M. tuberculosis) е основният и най-често срещан патоген, отговорен за туберкулозата (ТБ). Той може да попадне в човешкото тяло през дихателните пътища, храносмилателния тракт или увредена кожа и лигавици, заразявайки множество органи и причинявайки различни форми на ТБ. Белодробната ТБ, предавана предимно чрез капчици, представлява повече от 80% от случаите на ТБ. Честите симптоми включват кашлица, отделяне на храчки и хемоптиза. След инфекция в белите дробове, бактерията може да се разпространи чрез кръвния поток до множество системи, което потенциално може да доведе до скелетна, пикочна или стомашно-чревна ТБ.[2]
MTB е част от рода Mycobacterium, който включва:
- Mycobacterium tuberculosis complex (MTBC): Състои се от M. tuberculosis, M. bovis, M. africanum, M. canettii и M. microti, наред с други. Докато M. tuberculosis е основната причина за туберкулоза, M. bovis и M. africanum също могат да предизвикат заболяването.
- Нетуберкулозни микобактерии (НТМ).
- Mycobacterium leprae, причинителят на проказата.
Лабораторни диагностични подходи
Точната и навременна диагноза е от съществено значение за ефективния контрол на туберкулозата. Световната здравна организация подчертава, чеТехнологиите за бърза молекулярна диагностика коренно трансформираха откриването на туберкулоза, като позволиха високочувствителна и специфична идентификация на патогени, като същевременно откриват лекарствена резистентност.[1].
- Микроскопия и култураe: Културата остава златният стандарт за диагностициране на туберкулоза, тъй като позволява окончателно идентифициране на жизнеспособни организми и подпомага тестването за лекарствена чувствителност и геномния анализ. Въпреки това, поради бавния темп на растеж на Mycobacterium tuberculosis, резултатите обикновено изискват 2–8 седмици, което ограничава клиничната ѝ полезност при вземане на спешни решения.
-Имунологично изследване: Имунологичните методи, включително туберкулинов кожен тест (TST) и тестове за освобождаване на интерферон-гама (IGRA), откриват имунните отговори на гостоприемника към туберкулозна инфекция. Макар че са полезни за идентифициране на латентна инфекция, тези тестове не могат надеждно да разграничат активна от предходна инфекция и следователно имат ограничена диагностична специфичност в условия на висока заболеваемост.
-Молекулярна диагностика (NAAT): ДНК-базирани тестове, като например амплификация на нуклеинови киселини (NAAT), се препоръчват поради тяхната висока чувствителност и специфичност.
-Целенасочено секвениране от следващо поколение (tNGS): Технологиите за насочено секвениране осигуряват идентифициране с висока резолюция на мутациите, свързани с резистентност. Насоките на СЗО препоръчват tNGS като усъвършенстван инструмент за откриване на лекарствена резистентност след диагноза, подкрепящ прецизни стратегии за лечение [3].
-Метагеномно секвениране от следващо поколение (mNGS): Метагеномното секвениране позволява безпристрастно откриване на широк спектър от патогени без предварителен подбор на целта. Този подход е особено ценен при сложни или неясни клинични сценарии, включително смесени инфекции и имунокомпрометирани пациенти, където конвенционалната диагностика може да е недостатъчна.
СЗО допълнително подчертава, че микробиологичното потвърждение е от съществено значение за започване на подходяща терапия и подобряване на резултатите за пациентите, като по този начин засилва значението на интегрирането на съвременна молекулярна диагностика в програмите за контрол на туберкулозата [1].
Цялостни молекулярно-диагностични решения от Macro & Micro-Test
1.Мултиплексна PCR детекция за туберкулоза и лекарствена резистентностТуберкулоза
| Код на продукта | Име на продукта | Сертифициране |
| HWTS-RT001 | Комплект за откриване на ДНК на Mycobacterium Tuberculosis (флуоресцентна PCR) | CE |
| HWTS-RT137 | Комплект за откриване на мутации за резистентност към изониазид в Mycobacterium Tuberculosis (крива на топене) | CE |
| HWTS-RT074 | Комплект за откриване на резистентност към нуклеинова киселина и рифампицин на Mycobacterium Tuberculosis (крива на топене) | CE |
| HWTS-RT102 | Комплект за откриване на нуклеинови киселини, базиран на изотермична амплификация на ензимна сонда (EPIA) за Mycobacterium tuberculosis | CE |
| HWTS-RT144 | Комплект за откриване на нуклеинови киселини, замразени чрез изсушаване, на Mycobacterium Tuberculosis Complex (изотермична амплификация с ензимна сонда) | CE |
| HWTS-RT105 | Комплект за откриване на ДНК на лиофилизиран Mycobacterium Tuberculosis (флуоресцентна PCR) | CE |
| HWTS-RT147 | Комплект за откриване на резистентност към Mycobacterium Tuberculosis Nucleic Acid и Rifampicine, Isoniazid (крива на топене) | CE |
Когато има силно клинично съмнение за туберкулоза (ТБ),HWTS-RT147Тестът се препоръчва за качествено откриване на MTB инфекция и мултирезистентна туберкулоза (MDR-TB). Този тест идентифицира мутации вrpoB ген, които водят до резистентност към рифампицин (RIF), и мутации вгени katG и InhA, които са свързани с резистентност към изониазид (INH). Той осигурява ефикасен, еднократен тест както за MTB, така и за MDR-TB, включващ вътрешен контрол на качеството за минимизиране на фалшиво отрицателните резултати, осигурявайки бързи и точни резултати.
2.PTNseq насочено секвениране за респираторни патогени и профилиране на резистентност
| Код на продукта | Име на продукта | Спецификация. |
| HWKF-TS0001 | Комплект за обогатяване на гени на патогени на кръвна инфекция PTNseq | 24 теста/комплект |
| HWKF-TS0002 | Комплект за обогатяване на гени от патогенни микроорганизми на централната нервна система PTNseq | 24 теста/комплект |
| HWKF-TS0003 | Комплект за обогатяване на гени на респираторни инфекциозни патогени PTNseq | 24 теста/комплект |
| HWKF-AT0003 | Комплект за изграждане на автоматизирана библиотека за обогатяване (ONT) на PTNseq за патогенни микроорганизми при респираторни инфекции | 24 теста/комплект |
| HWKF-TS0004 | PTNseq Комплект за обогатяване на гени с широк спектър на инфекциозни патогени | 24 теста/комплект |
| HWKF-TS0005 | PTNseq Комплект за обогатяване на гени от ултраширокоспектърни инфекциозни патогенни микроорганизми | 24 теста/комплект |
| HWKF-TS0151 | Комплект за генно обогатяване на микобактерии и лекарствена резистентност (метод на множествена амплификация) | 24 теста/комплект |
В случаи на смесени респираторни инфекции (включително инфекции на горните и долните дихателни пътища, туберкулоза и хронични респираторни заболявания) или когато е необходим анализ на гени за лекарствена резистентност (напр. съмнение за лекарствено-резистентна туберкулоза),PTNseq серия от целенасочено високопроизводително генно откриванеможе да се приложи. Базиран на усъвършенствана технология за таргетирано секвениране, PTNseq използва ултра-мултиплексна PCR за обогатяване на специфични целеви последователности, комбинирана с високопроизводително секвениране и технология от трето поколение нанопори за цялостна идентификация на патогени и профилиране на лекарствена резистентност.
Системата използва патентовани, високоспецифични праймери за ултра-мултиплексна амплификация на целеви гени. Поддържана от собствена база данни и интелигентни биоинформатични алгоритми, тя осигурява точна идентификация на патогени, заедно с анализ на гени за лекарствена резистентност и вирулентност. Целенасоченото обогатяване намалява интерференцията от ДНК на гостоприемника, подобрявайки чувствителността в проби с висок човешки произход и позволявайки ефективно откриване на трудни цели, като напримерМикобактериум туберкулоза, гъбички, вътреклетъчни бактерии, РНК вируси и гени за резистентност или вирулентност.
PTNseq достига граница на откриванеедва 100 копия/мли покрива175 често срещани респираторни патогени, включително 76 бактерии, 73 вируса, 19 гъбички, 7 микоплазми, както иХламидия, Рикетсияи 54 гена за лекарствена резистентностПанелът включваМикобактериум туберкулозасложни и основни нетуберкулозни микобактерии.
Серията PTNseq съчетава висока чувствителност с рентабилност, подобрявайки нивата на откриване на патогени и поддържайки индивидуализирана антимикробна терапия, като същевременно спомага за намаляване на антимикробната резистентност. Интегрирана с напълно автоматизираната система за подготовка на библиотеки за генно секвениране (AIOS), тя предоставя рационализирано решение в болница с време за обработка от едва 6,5 часа от пробата до резултата.

3. Метагеномно секвениране за широкоспектърно откриване на патогени
| Код на продукта | Име на продукта | Спецификация. |
| HWKF-MN0011 | Комплект за откриване на метагеномни патогени (DNA-Illumina) | 24 теста/комплект |
| HWKF-MN0018 | Комплект за откриване на метагеномни патогени (DNA-MGI) | 24 теста/комплект |
| HWKF-MN0021 | Комплект за откриване на метагеномни патогени (DNA-ONT) | 24 теста/комплект |
| HWKF-MN0012 | Комплект за откриване на метагеномни патогени (RNA-Illumina) | 24 теста/комплект |
| HWKF-MN0019 | Комплект за откриване на метагеномни патогени (RNA-MGI) | 24 теста/комплект |
| HWKF-MN0022 | Комплект за откриване на метагеномни патогени (RNA-ONT) | 24 теста/комплект |
| HWKF-MN0013 | Комплект за откриване на метагеномни патогени (ДНК+РНК-Illumina) | 24 теста/комплект |
| HWKF-AYM0013 | Комплект за автоматизирано изграждане на библиотеки за откриване на метагеномни патогени (ДНК+РНК-Илумина) | 24 теста/комплект |
| HWKF-MN0020 | Комплект за откриване на метагеномни патогени (ДНК+РНК-MGI) | 24 теста/комплект |
| HWKF-MN0023 | Комплект за откриване на метагеномни патогени (ДНК+РНК-ОНТ) | 24 теста/комплект |
Когато клиничната диагноза е неясна,mNGS патогенно високопроизводително откриване на гениможе да се извърши върху различни проби от пациента, включително бронхоалвеоларен лаваж, храчки, тампони от гърлото, кръв, плеврален излив, гной и тъканни проби. Този подход използва технология за метагеномно секвениране, при която различни проби се подлагат на целенасочена предварителна обработка, последвана от екстракция на нуклеинови киселини с помощта на стъклени перли и ензими, разграждащи стените, което повишава ефективността на екстракцията. Секвенирането е адаптирано към множество платформи, осигурявайки голям обем данни за подобрена чувствителност на mNGS и целостта на сглобяването. Данните се анализират с помощта на самостоятелно изградена база данни и интелигентни алгоритми за откриване.над 20 000 патогена, включително бактерии, гъбички, вируси и паразити, предоставяйки информация за предполагаеми патогенни микроорганизми. Този метод е подходящ за трудни за диагностициране, критично болни или имунокомпрометирани пациенти, включително идентифициране наПланинско колоезденекомплексиНТМ, както и смесени инфекции. Това значително подобрява нивата на откриване на патогени и помага за насочване на клинично насочената употреба на антибиотици, което позволява прецизна диагностика на инфекциите.
Заключение
Въпреки постигнатия значителен напредък, туберкулозата остава основно глобално здравно предизвикателство, особено в контекста на лекарствената резистентност, недостига на финансиране и неравния достъп до диагностика.
СЗО подчертава, че разширяването на достъпа до бърза молекулярна диагностика и усъвършенствани технологии за секвениране е от съществено значение за постигане на целите на Стратегията за премахване на туберкулозата. С непрекъснати иновации, инвестиции и глобално сътрудничество, премахването на туберкулозата вече не е просто желание, а постижима цел.
Референции:
- Световна здравна организация. Глобален доклад за туберкулозата 2024/2025: Диагностично изследване и лечение.
- Световна здравна организация. Ръководство на СЗО за избор на молекулярни бързи диагностични тестове, препоръчани от СЗО, за откриване на туберкулоза и лекарствено-резистентна туберкулоза.
- Световна здравна организация. Консолидирани насоки на СЗО за туберкулоза: Модул 3 – Диагноза (Актуализация 2024 г.).
Време на публикуване: 24 март 2026 г.
